11.CO2で実験しよう |
| もくじへ |
| [目的] | 二酸化炭素を使いさまざまな化学実験を行う。 |
| [領域] | 物理:気体の密度 化学:物質の変化 |
| 1. | CO2でシャボン玉を浮かす | |
| [準備] | 石灰石(炭酸カルシウムCaCO3) 塩酸HCl シャボン液 ストロー 容器(1リットル ビーカー 水槽など) | |
| [操作] |
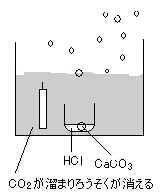
| 1) | 石灰石と塩酸で二酸化炭素を発生させ、容器中に貯める。 |  | ||
| 2) | 容器の中にシャボン玉を吹き込む。 | |||
| [留意点・工夫点] | ||||
| ・ | 容器の中にろうそくを立てておくと炎が消えることで二酸化炭素が溜まったことを確認できる。ドライアイスを使用してもよい。 | |||
| ・ | 二酸化炭素の密度が空気より大きいことにより、シャボン玉はビーカーの途中に浮いたままの状態になる。 | |||
| ・ | この実験は、空気より重い二酸化炭素CO2中でシャボン玉を浮かせ、気体密度の違いを確認するものである。 | |||
| 2. | CO2中でマグネシウムリボンを燃やす | |
| [準備] | 二酸化炭素CO2 マグネシウムMgリボン | |
| [操作] |
| 二酸化炭素を容器中に貯め、点火したマグネシウムリボンを入れる。 |
| [留意点・工夫点] | ||
| ・ | マグネシウムリボンは空気中では白光を出し静かに燃えるが、二酸化炭素中ではパチパチと音をたてて燃える。 | |
| ・ | マグネシウムリボンに火をつけて、ドライアイスではさみ燃焼を観察する方法もある。マグネシウムリボンを入れられるよう、ドライアイスをくりぬいておく。 | |
| ・ | 空気中で燃焼の場合 2Mg+O2→2MgO
二酸化炭素中で燃焼の場合 2Mg+CO2→2MgO+C CO2の結合よりMgとO2の結合のほうが強い。 | |
| もくじへ |