24.中和滴定曲線
| [目的] | 酸に塩基(塩基に酸)を加えて中和していくときのpHの変化を調べる。 |
| [薬品・材料] | |
| 塩酸HCl 水酸化ナトリウムNaOH フェノールフタレイン 万能pH試験紙 | |
| [器具] | ビュレット コニカルビーカー ホールピペット ガラス棒 ガラス板(アクリル板) セロハンテープ |
| [操作] | |
| 1) | 「中和滴定」の操作に準ずる。 |
| 2) | 一定量ずつ滴下させるごとによくかき混ぜ、ガラス棒で万能pH試験紙にしみ込ませ液性を調べる。 |
| 3) | pHの値をグラフに表す。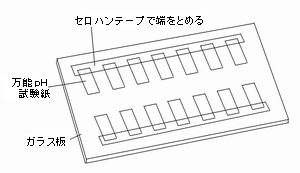 |
 |
||
| [留意点・工夫点] | ||
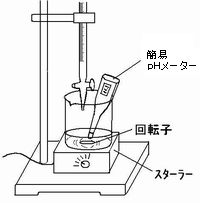
| ★ | 万能pH試験紙の代わりにpHメーターを用いて直接pHを読みとってもよい。pHメーターを用いて滴定する場合、マグネティックスターラーで撹拌しながら水酸化ナトリウム水溶液を滴下する方法もある。 | |
| ★ | 薬品・器具に関する注意は、「酸と塩基」、「中和滴定」を参照。 | |
| <参考> | ||
| 中和における指示薬の選択 | ||
| ① | 強酸と弱塩基(例:塩酸とアンモニア水) ・・・中和点は酸性側。 |
|
| ② | 弱酸と強塩基(例:酢酸と水酸化ナトリウム) ・・・中和点は塩基性側。 |
|
| ③ | 強酸と強塩基(例:塩酸と水酸化ナトリウム) ・・・中和点はpH7付近でpHの変化は酸性側、塩基性側にわたる。 |
|
| ④ | 弱酸と弱塩基(例:酢酸とアンモニア水) ・・・中和点はpH7付近であるが、変化の範囲が狭く、薬品の種類によって中和点 のpHも変化するので、適当な指示薬を決めることができない。 |
|