52.ベンゼンの性質と置換反応
| [目的] | ベンゼンからニトロベンゼン、ベンゼンスルホン酸ナトリウムを合成し、ベンゼンでは置換反応が起こりやすいことを調べる。 |
| [薬品] | ベンゼン 濃硫酸 濃硝酸 エタノール ジエチルエーテル 水酸化ナトリウム 希塩酸 塩化ナトリウム 過マンガン酸カリウム 臭素水 鉄粉 |
| [器具] | 蒸発皿 吸引ろ過装置 |
| [操作] | |
| 1) | ベンゼンの性質 |
| ① | ベンゼンを試験管にとり、色・においなどを調べる。次に水を加えよく振って静置し、水溶性を調べる。 |
| ② | ベンゼンに点火し、炎の色や燃え方などを観察する。 |
| ③ | 2本の試験管にベンゼンをとり、それぞれ硫酸酸性過マンガン酸カリウムや臭素水を加えてよく振り混ぜ変化を見る。 |
| 2) | ベンゼンの置換反応 |
| a. | ベンゼンのニトロ化(ニトロベンゼンの合成) |
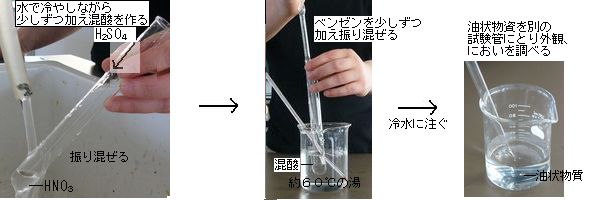
| ① | 濃硝酸に濃硫酸を水で冷やしながら少しずつ加えて混酸を作る。混酸にベンゼンを加えてよく振り、約60℃で暖めるとニトロベンゼンが生成する。 |
| ② | 冷水に注ぐと油状物のニトロベンゼンが沈むので、これをスポイトで試験管にとり、生成物の外観やにおいを調べる。 |
| ③ | できたニトロベンゼンをエタノール・塩酸・ジエチルエーテル・ベンゼン・水酸化ナトリウムが入っているそれぞれの試験管に入れ、溶けるかを調べる。 |
 |
|
| b. | ベンゼンのスルホン化(ベンゼンスルホン酸ナトリウムの合成) |
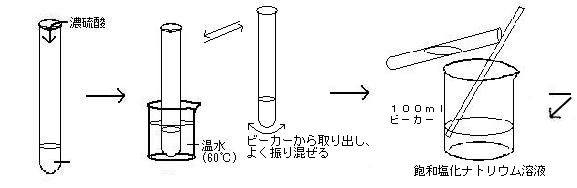
| ① | ベンゼンに濃硫酸を加え、約60℃で暖めるとベンゼンスルホン酸が生成する。これを飽和塩化ナトリウム溶液を入れたビーカーに注ぎ込むと沈殿(塩化ナトリウム)が生じる。 |
| ② | 1で生じた沈殿を除くため、ビーカー内の溶液を熱いうちに吸引ろ過し、ろ液をビーカーに移し氷水で冷却すると結晶(ベンゼンスルホン酸ナトリウム)が析出する。 |
 |
|
 |
|
| c. | ベンゼンのハロゲン化 |
| ベンゼンに臭素を溶かし、鉄粉(触媒)を加えて暖めるとブロモベンゼンが生成する。 | |
| [留意点・工夫点] | |
| ☆ | ベンゼンは発ガン性物質であるので、深く吸入しないように注意する。 |
| ☆ | 濃硫酸は空気中の水分を吸って薄くなっていることがあるので、新しいものを使用する。 |
| ☆ | 濃硝酸に濃硫酸を加えたりベンゼンを加える時水で冷やすのは、温度が高くなる(80℃以上)とベンゼンが蒸発したり、ニトロ化が進んでジニトロベンゼンができるためである。50~60℃の状態で時々よく振り混ぜてやるとニトロベンゼンが多量にできる。 |
| ☆ | 硝酸の量が多かったり温度が少し高いと、反応液は赤くなるが、そのまま続けてよい。 |
| ☆ | ニトロベンゼンはビーカーの底で丸い油滴状となる。上に浮いているのは未反応のベンゼンである。油滴をなるべくひとまとめにしてスポイトで吸い上げるには、あまり水を捨ててしまわない方がやりやすい。 |
| ☆ | bの実験で飽和塩化ナトリウム水溶液に注ぐときは、反応が激しく液が飛び散る場合があるので少しずつ注ぐ。 |
| ☆ | 生成物の収量は温度が低いほど多くなるので、氷水でかなり冷やす方がよい。シャーベット状になったものをもう一度吸引ろ過すると生成物が確認できる。 |
| ☆ | ジエチルエーテルの蒸気は引火性が強く、麻酔作用があるので気をつける。 |
| ★ | 先端を細長くしたスポイトを使用するとニトロベンゼンを集めやすい。 |